Θεραπεία και Καινοτομία
Τα τελευταία χρόνια έχει υπάρξει σημαντική πρόοδος στο πεδίο της ιατρικής έρευνας και της μοριακής βιολογίας όσον αφορά τον καρκίνο του πνεύμονα. Πλέον, οι κλασσικές θεραπείες όπως η χημειοθεραπεία δεν είναι η μόνη θεραπευτική επιλογή. Οι θεραπευτικές επιλογές είναι αρκετές και εξατομικεύονται ανάλογα με τα μοναδικά χαρακτηριστικά του κάθε ασθενή και τη βιολογία του όγκου.

Χειρουργική προσέγγιση
-
–
Πριν την επέμβαση
Ο ασθενής που είναι υποψήφιος για χειρουργείο πρέπει αρχικά να υποβληθεί σε προεγχειρητικό έλεγχο, ώστε να διαπιστωθεί ότι η κατάσταση της υγείας του είναι αρκετά καλή ώστε να ανταπεξέλθει στο χειρουργείο. Ο προεγχειρητικός έλεγχος περιλαμβάνει:
- Γενικές εξετάσεις. Πρέπει να πραγματοποιηθεί μια σειρά απλών εξετάσεων όπως η γενική εξέταση αίματος και ο πλήρης βιοχημικός και έλεγχος πηκτικότητας του αίματος. Απαραίτητο είναι να ελεγχθεί η καρδιακή λειτουργία με ηλεκτροκαρδιογράφημα και εκτίμηση από καρδιολόγο.
- Έλεγχος της αναπνευστικής λειτουργίας. Αποτελεί καθοριστική εξέταση διότι προσδιορίζει τη δυνατότητα για επαρκή αναπνευστική λειτουργία μετά την αφαίρεση τμήματος ή και ολόκληρου του πνεύμονα. Ασθενείς με προϋπάρχοντα αναπνευστικά προβλήματα μπορεί να εκτιμηθεί ότι δεν μπορούν να εξασφαλίσουν επαρκή αναπνευστική λειτουργία μετά το χειρουργείο και ο ογκολόγος να τους προτείνει μια εναλλακτική θεραπευτική αντιμετώπιση που θα τους εξασφαλίσει την καλύτερη δυνατή ποιότητα ζωής.
- Απεικονιστικές εξετάσεις. Η προεγχειρητική σταδιοποιήση με τη χρήση απεικονιστικών εξετάσεων όπως αξονικές τομογραφίες, μαγνητικές τομογραφίες, σπινθηρογράφημα οστών, PET scanning κλπ πραγματοποιούνται προκειμένου να προσδιοριστεί η έκταση-στάδιο της νόσου, η ανατομική θέση του όγκου και συνεπώς η θεραπεία εκλογής για κάθε ασθενή.
- Ιστολογική επιβεβαίωση του ΚΠ. H προεγχειρητική τεκμηρίωση του ΚΠ με τη λήψη βιοψιών με ελάχιστα επεμβατικές τεχνικές αποτελεί τη συνήθη τακτική. Η προεγχειρητική τεκμηρίωση του ιστολογικού τύπου είναι απαραίτητη για τον σχεδιασμό των θεραπευτικών επιλογών. Σε λιγότερες περιπτώσεις, όταν η ιστολογική επιβεβαίωση είναι ανέφικτη προεγχειρητικά, αυτό γίνεται κατά τη διάρκεια της χειρουργικής επέμβασης.
Σε μία μικρή υποομάδα ασθενών με μη μικροκυτταρικό ΚΠ μπορεί να χρειαστεί χορήγηση χημειοθεραπείας πριν από το χειρουργείο. Ο λόγος είναι να συρρικνωθούν οριακά μη χειρουργήσιμοι τοπικά εκτεταμένοι όγκοι ώστε να μπορούν να εξαιρεθούν πλήρως. Η εξατομικευμένη προσέγγιση του ασθενούς από τον ειδικό ιατρό θα βοηθήσει στον σωστό σχεδιασμό της θεραπείας του.
Κατά τη διάρκεια της επέμβασης
Σε κάθε περίπτωση, η χειρουργική επέμβαση για την αντιμετώπιση του ΚΠ απαιτεί την χορήγηση γενικής αναισθησίας στον ασθενή. Υπάρχουν τρεις κύριοι τύποι επεμβάσεων:
Τμηματεκτομή είναι η αφαίρεση ενός μικρού τμήματος του πνεύμονα μέσα στο οποίο εμπεριέχεται ο όγκος.
Λοβεκτομή είναι η αφαίρεση ενός λοβού του πνεύμονα. Είναι η πιο συχνή επέμβαση για περιορισμένη νόσο.
Πνευμονεκτομή είναι η αφαίρεση του ενός πνεύμονα.
Η επιλογή κάθε φορά του τύπου της επέμβασης εξαρτάται από παράγοντες που μπορούν να προσδιοριστούν εν μέρει προεγχειρητικά π.χ. οι αναπνευστικές εφεδρείες αλλά και διεγχειρητικά (δηλ. κατά τη διάρκεια του χειρουργείου). Έτσι, είναι δυνατόν ο χειρουργός κατά τη διάρκεια της επέμβασης να τροποποιήσει τον αρχικό σχεδιασμό εάν διαπιστώσει ότι η νόσος είναι περισσότερο εκτεταμένη από ότι είχε προσδιοριστεί με τον προεγχειρητικό απεικονιστικό έλεγχο. Σε κάθε περίπτωση ο στόχος είναι η πλήρης εξαίρεση του όγκου με την μικρότερη δυνατή απώλεια πνευμονικού παρεγχύματος.
Μετά την επέμβαση
Κατά την μετεγχειρητική ανάρρωση ο ασθενής θα διαπιστώσει ότι φέρει στο θώρακα του κάποιες παροχετεύσεις (σωληνάκια) που ο ρόλος τους είναι να απομακρύνουν αίμα και σωματικά υγρά από την περιοχή του τραύματος. Οι παροχετεύσεις αυτές θα απομακρυνθούν όταν δεν θα έχουν πλέον περιεχόμενο, περίπου σε 7 ημέρες. Εξετάσεις αίματος, ακτινογραφίες θώρακος, χορήγηση αντιβιοτικής αγωγής για την αντιμετώπιση λοιμώξεων αποτελούν μέρος της μετεγχειρητικής περιόδου εξατομικευμένα για κάθε ασθενή.
Όσον αφορά την δύσπνοια μετά την επέμβαση, ο θεράπων ιατρός θα ζητήσει να γίνουν προεγχειρητικά διάφορες εξετάσεις ελέγχου της αναπνευστικής λειτουργίας που θα καθοδηγήσουν τον χειρουργό στο να αποφασίσει ποιος τύπος επέμβασης είναι ο πιο κατάλληλος για τον κάθε ασθενή. Ασθενείς με ιστορικό αναπνευστικής νόσου ίσως χρειαστούν μια επιπρόσθετη φροντίδα. Αναπνευστικές ασκήσεις με την βοήθεια φυσιοθεραπευτή θα βοηθήσουν να αποκτήσουν σταδιακά επαρκή αναπνευστική λειτουργία.
Ο πόνος αποτελεί ίσως την μεγαλύτερη ανησυχία των ασθενών που υποβάλλονται σε μια θωρακοχειρουργική επέμβαση. Ο πόνος είναι υπαρκτός τις πρώτες ημέρες μετά το χειρουργείο. Όμως ο ιατρός έχει στην διάθεση του ένα μεγάλο αριθμό αναλγητικών φαρμάκων που μπορεί να χρησιμοποιήσει ώστε να εξασφαλίσει στον ασθενή μια ανώδυνη μετεγχειρητική ανάρρωση αρκεί ο ασθενής να συνεργαστεί μαζί του. Πιο σπάνια, κάποιοι ασθενείς αντιμετωπίζουν το αίσθημα του πόνου εβδομάδες ή μήνες μετά το χειρουργείο που μπορεί να οφείλεται στον τραυματισμό κάποιου νεύρου κατά τη διάρκεια της επέμβασης. Ο πόνος αυτός μπορεί να παρουσιάσει ύφεση – εάν όμως παραμένει, μπορεί ο ασθενής να συμβουλευτεί ένα ιατρείο πόνου.
Συνήθως ο ασθενής μπορεί να επιστρέψει στο σπίτι σε 2 εβδομάδες. Η ανάρρωση του κάθε ασθενούς εξαρτάται από πολλούς παράγοντες και δεν μπορεί να προσδιοριστεί με ακρίβεια. Η προεγχειρητικά καλή γενική κατάσταση, το νεαρό της ηλικίας, η γρήγορη κινητοποίηση, η συνεργασία με φυσιοθεραπευτή αποτελούν ευνοϊκούς παράγοντες μιας καλής και ταχείας μετεγχειρητικής πορείας.
Σε κάποιους ασθενείς, ανάλογα με την έκταση της νόσου όπως αυτή διαπιστώθηκε τόσο πριν όσο και κατά τη διάρκεια του χειρουργείου, είναι απαραίτητη η χορήγηση επικουρικής χημειοθεραπείας ή και ακτινοθεραπείας. Αυτό κρίνεται από τον θεράποντα ογκολόγο με βάση την ιστολογική εξέταση που προέκυψε από το χειρουργείο και τις απεικονιστικές εξετάσεις.
Χημειοθεραπεία
Έναρξη χημειοθεραπευτικών κύκλων
Τα κυτταροστατικά φάρμακα συνήθως χορηγούνται από τη φλέβα (ενδοφλέβια έγχυση), αλλά ορισμένα από αυτά μπορούν να ληφθούν και από το στόμα. Η χημειοθεραπεία, ανάλογα με τον συνδυασμό των φαρμάκων και τις δόσεις τους επαναλαμβάνεται συνήθως κάθε δύο ή τρεις εβδομάδες. Ενδιάμεσα παρεμβάλλονται διαστήματα χωρίς θεραπεία για να δίνεται στον οργανισμό η ευκαιρία να αναρρώνει από τις παρενέργειες. Η συνολική διάρκεια της θεραπείας, δηλαδή πόσα σχήματα συνολικά θα γίνουν εξαρτάται από τον τύπο του καρκίνου και από την ανταπόκριση στα φάρμακα.
Ομάδα από ειδικούς ιατρούς πολλών ειδικοτήτων παίρνει την απόφαση για την κατάλληλη θεραπεία, που πρέπει να χορηγηθεί σε έναν ασθενή. Ο Παθολόγος –
Ογκολόγος είναι εκείνος που θα διαμορφώσει την τελική μορφή της θεραπείας: τον πιο αποτελεσματικό συνδυασμό κυτταροστατικών φαρμάκων, που θα χορηγηθούν ανάλογα με την περίπτωση της νόσου του ασθενούς, τη χρονική σειρά που πιθανόν θα εφαρμοστεί η χειρουργική ή/και η ακτινοθεραπεία, τη χρονική στιγμή έναρξης της θεραπείας και τη διάρκειά της, καθώς και την παρακολούθηση της ανταπόκρισης της νόσου σε αυτήν και την αντιμετώπιση των ανεπιθύμητων ενεργειών.
Συνήθως, η χημειοθεραπεία χορηγείται σε οργανωμένες Ογκολογικές Μονάδες Ημερήσιας Νοσηλείας, όπου οι ασθενείς λαμβάνουν τη θεραπεία ενδοφλεβίως και εξέρχονται της Κλινικής με το πέρας της έγχυσης. Ωστόσο, σε ορισμένες περιπτώσεις χημειοθεραπευτικών σχημάτων, η έγχυση γίνεται επί 18 ή 22 ωρών συνεχώς, οπότε η νοσηλεία του ασθενούς είναι απαραίτητη.
Ανεπιθύμητες ενέργειες
Οι πιο συχνές και συνηθισμένες ανεπιθύμητες ενέργειες της χημειοθεραπείας είναι η ναυτία και ο έμετος, τα οποία όμως προλαμβάνονται και αντιμετωπίζονται, όταν εμφανιστούν, με ειδική αντιεμετική αγωγή. Πρέπει να σημειωθεί ότι δεν είναι όλα τα φάρμακα εμετογόνα στον ίδιο βαθμό. Μερικά φάρμακα προκαλούν μικρά έλκη στη στοματική κοιλότητα, γι’ αυτό και απαιτείται πλύσιμο του στόματος συχνά με αντισηπτικό. Κόπωση σε μικρή προσπάθεια και καταβολή είναι επίσης συχνές ανεπιθύμητες ενέργειες των κυτταροστατικών φαρμάκων. Ορισμένοι ασθενείς συνεχίζουν να έχουν τη συνηθισμένη, καθημερινή τους δράση, ενώ άλλοι μειώνουν τις δραστηριότητές τους προκειμένου να ανταπεξέλθουν στις νέες συνθήκες διαβίωσης. Ο ασθενής με καρκίνο, που λαμβάνει χημειοθεραπεία είναι περισσότερο ευάλωτος στις λοιμώξεις. Όποτε θεωρείται σκόπιμο, συστήνονται αιματολογικές εξετάσεις από τον θεράποντα ιατρό για τον έλεγχο του αιματοκρίτη, των λευκών αιμοσφαιρίων και των αιμοπεταλίων. Αν η θερμοκρασία του σώματος ανέβει πάνω από τους 38ο C, τότε πρέπει να ενημερωθεί ο ιατρός το συντομότερο δυνατόν. Η απώλεια των μαλλιών είναι συνηθισμένο φαινόμενο κατά τη διάρκεια της χημειοθεραπείας. Λίγους μήνες μετά το πέρας της θεραπείας, ο ασθενής έχει και πάλι κανονικά και υγιή μαλλιά. Διαφορετικές κατά περίπτωση εκδηλώσεις από το γαστρεντερικό σύστημα, όπως είναι η δυσκοιλιότητα ή οι διαρροϊκές κενώσεις αντιμετωπίζονται με ειδική αγωγή, που θα χορηγήσει ο ιατρός. Ο ιατρός θα προσπαθήσει να προλάβει ένα μεγάλο ποσοστό των ανεπιθύμητων ενεργειών της χημειοθεραπείας και της ακτινοθεραπείας. Αν ωστόσο αυτό δεν γίνει τελικά εφικτό και για όσο διάστημα εφαρμόζεται η θεραπεία, υπάρχουν ποικίλοι τρόποι και ειδικά φάρμακα είτε με τη μορφή χαπιών είτε ως ενέσεις, με τα οποία αντιμετωπίζονται επιτυχώς οι ανεπιθύμητες ενέργειες.
Μετά το τέλος των χημειοθεραπειών
Μετά το πέρας των θεραπειών οι περισσότερες ανεπιθύμητες ενέργειες σταματούν. Ορισμένες, όπως, για παράδειγμα, τα μουδιάσματα στα χέρια και τα πόδια μπορεί να κρατήσουν για μερικούς μήνες. Τα μαλλιά φυτρώνουν ξανά μέσα σε περίοδο 3-6 μηνών μετά τη θεραπεία.
Επειδή υπάρχει κίνδυνος υποτροπής του καρκίνου στην ίδια εστία που είχε παρουσιαστεί αρχικά ή κάπου αλλού στο σώμα, επιβάλλεται, μετά την ολοκλήρωση των κύκλων της χημειοθεραπείας, η τακτική παρακολούθηση του ασθενούς από τον θεράποντα ιατρό, με σκοπό την έγκαιρη ανίχνευση της επανεμφάνισης του όγκου.
Πριν την αναχώρησή του ασθενούς από την Ογκολογική Μονάδα Ημερήσιας Νοσηλείας ή το Νοσοκομείο, θα του δοθεί ραντεβού για την επίσκεψή του στα εξωτερικά ιατρεία για τις τακτικές αιματολογικές εξετάσεις και τον έλεγχο ρουτίνας με απεικονιστικές εξετάσεις. Αυτό θα συνεχιστεί για μερικά χρόνια, αρχικά ανά συχνά χρονικά διαστήματα, τα οποία μετά την παρέλευση της πενταετίας θα γίνουν αραιότερα. Στα χρονικά διαστήματα από το ένα ραντεβού έως το επόμενο, τυχόν νέα συμπτώματα ή προβλήματα θα πρέπει να αναφερθούν στον ιατρό.

Σταδιοποίηση
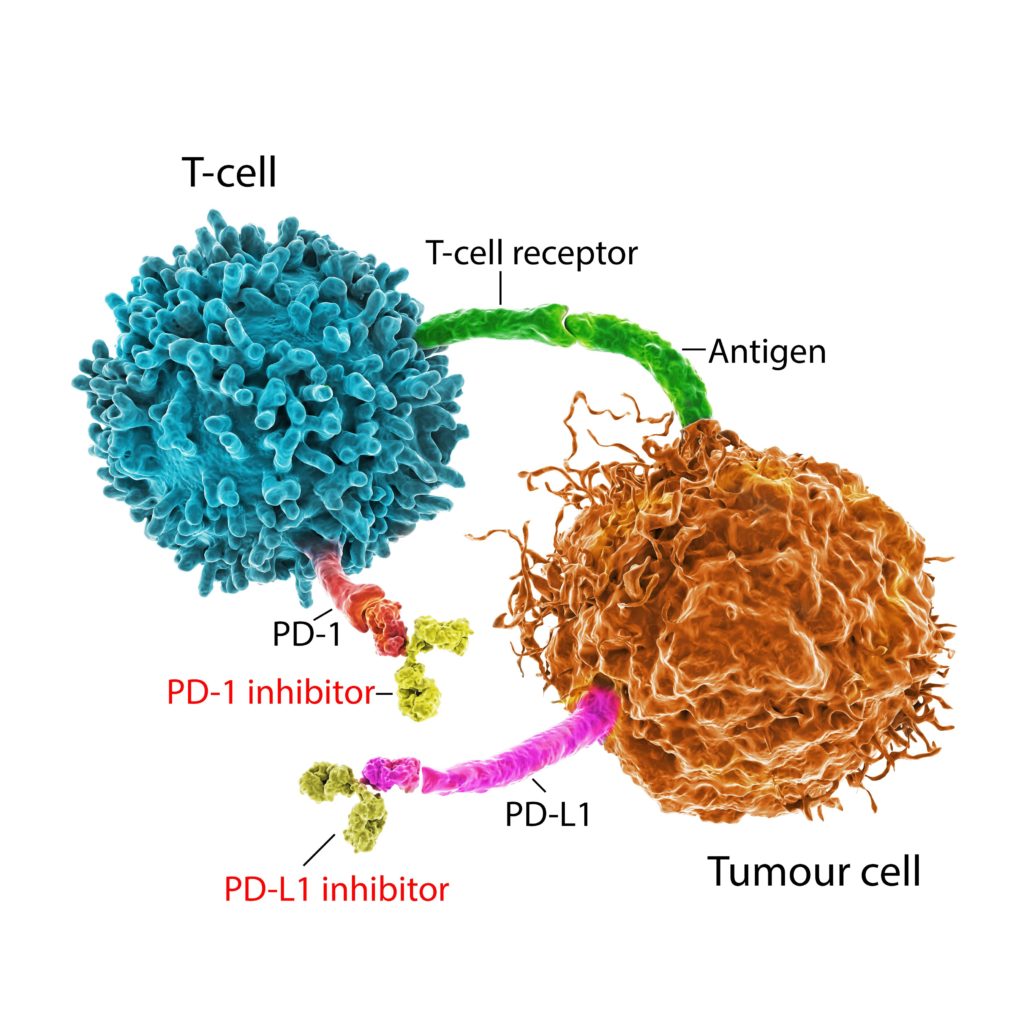
Στοχευμένες θεραπείες
Tα τελευταία χρόνια η γνώση της βιολογίας του καρκίνου του πνεύμονα έχει εξελιχθεί, προσφέροντας νέες δυνατότητες σε διαγνωστικό και θεραπευτικό επίπεδο. Με τον όρο «στοχευμένες θεραπείες» στον καρκίνο πνεύμονα εννοούμε θεραπείες που στοχεύουν σε συγκεκριμένες πρωτεΐνες και γονίδια που εμπλέκονται στην ανάπτυξη και την επιβίωση των καρκινικών κυττάρων. Οι στοχευμένες θεραπείες μπορεί να επηρεάζουν το περιβάλλον στο οποίο αναπτύσσονται και επιβιώνουν τα καρκινικά κύτταρα ή κύτταρα στόχους που σχετίζονται με την ανάπτυξη του όγκου, όπως τα κύτταρα των αγγείων.
Τα γονίδια σε όλα τα φυσιολογικά κύτταρα του οργανισμού δίνουν το μήνυμα για την παραγωγή πρωτεϊνών που είναι υπεύθυνες, μεταξύ άλλων, για τον κύκλο ζωής του κυττάρου. Σε κάποιες περιπτώσεις υπάρχει μία αλλαγή στα γονίδια αυτά (γενετική μετάλλαξη) με αποτέλεσμα να δίνεται λανθασμένο σήμα στο κύτταρο και να υπάρχουν αλλαγές στις πρωτεΐνες που παράγονται. Αυτό έχει ως αποτέλεσμα το κύτταρο να αναπαράγεται πολύ γρήγορα και να επιβιώνει πολύ περισσότερο, μετατρεπόμενο σε καρκινικό κύτταρο. Τα κύτταρα αυτά βγαίνουν εκτός ελέγχου και έτσι δημιουργείται ο καρκινικός όγκος.
Τα τελευταία χρόνια έχουν αναπτυχθεί διάφορες στοχευμένες θεραπείες έναντι κυτταρικών στοιχείων ανάλογα με τον ιστολογικό τύπο και τα ειδικά χαρακτηριστικά του όγκου. Για να διαπιστωθεί αν ένας συγκεκριμένος όγκος είναι ευαίσθητος σε αυτά τα φάρμακα θα πρέπει να γίνει μία ειδική εξέταση στα κύτταρα του όγκου (μοριακός έλεγχος). Είναι πολύ πιθανό όμως κατά τον μοριακό έλεγχο να μην διαπιστωθεί κάποια μετάλλαξη για την οποία να υπάρχει στοχευμένη θεραπεία. Σε αυτήν την περίπτωση ο ασθενής θα πρέπει να λάβει κλασσική χημειοθεραπεία και/ή ανοσοθεραπεία.
Φάρμακα τα οποία στοχεύουν στην ανάπτυξη αγγειακού δικτύου στον όγκο (αγγειογένεση)
Η ανάπτυξη ενός όγκου προϋποθέτει την αγγείωσή του ώστε να μπορεί να τραφεί και να μεγαλώνει. Υπάρχουν φάρμακα τα οποία ανήκουν στην κατηγορία των μονοκλωνικών αντισωμάτων που στοχεύουν στο να εμποδίσουν την ανάπτυξη νέων αγγείων (αγγειογένεση) στον όγκο. Τα μονοκλωνικά αντισώματα γενικά είναι μόρια, τα οποία είναι σχεδιασμένα κατά τέτοιο τρόπο, ώστε να προσκολλώνται σε συγκεκριμένους κυτταρικούς υποδοχείς στην επιφάνεια του κυττάρου και να εμποδίζουν την ενεργοποίησή τους. Οι υποδοχείς αυτοί υπό φυσιολογικές συνθήκες όταν ενεργοποιούνται δίνουν σήμα στο κύτταρο να εκτελέσει μία συγκεκριμένη λειτουργία. Τα μονοκλωνικά αντισώματα εμποδίζουν την ενεργοποίηση των υποδοχέων και άρα την εκτέλεση της συγκεκριμένης λειτουργίας. Στη θεραπεία του καρκίνου του πνεύμονα, τα μονοκλωνικά αντισώματα έχουν ως στόχο τον αγγειακό ενδοθηλιακό αυξητικό παράγοντα και δρουν στα ενδοθηλιακά κύτταρα των αγγείων με αποτέλεσμα να παρεμποδίζεται η ανάπτυξη νέων αιμοφόρων αγγείων, να αποκόπτεται η τροφοδοσία του όγκου με αίμα και κατ’ επέκταση η αύξηση και εξάπλωσή του.
Θεραπείες που στοχεύουν μεταλλάξεις στο γονίδιο EGFR (αναστολείς της τυροσινικής κινάσης)
Ο υποδοχέας του επιδερμικού αυξητικού παράγοντα (EGFR) είναι μία πρωτεΐνη στην επιφάνεια των κυττάρων που βοηθάει την ανάπτυξη και τον πολλαπλασιασμό τους. Σε κάποιες περιπτώσεις αδενοκαρκινωμάτων πνεύμονα, μία μετάλλαξη που κωδικοποιεί το γονίδιο EGFR προκαλεί την υπερπαραγωγή του με αποτέλεσμα τον ανεξέλεγκτο κυτταρικό πολλαπλασιασμό. Οι αναστολείς τυροσινικής κινάσης (TKIs) είναι μία ομάδα φαρμάκων που αναστέλλει το σήμα του EGFR το οποίο δίνει εντολή στο κύτταρο για πολλαπλασιασμό και έτσι αναστέλλει και την ανάπτυξη του όγκου.
Θεραπείες που στοχεύουν μεταλλάξεις σε άλλα γονίδια
Σε ακόμα πιο σπάνιες περιπτώσεις υπάρχουν κάποιες μεταλλάξεις σε διαφορετικά γονίδια που σχετίζονται με την καρκινογένεση και την λειτουργία καρκινικού κυττάρου (πχ ALK, BRAF, ROS1 κα). Για κάποιες από αυτές έχουν αναπτυχθεί στοχευμένες θεραπείες που βοηθούν στον έλεγχο της νόσου και στη συρρίκνωση του όγκου.
Η έρευνα στον τομέα της μοριακής βιολογίας του καρκίνου του πνεύμονα εξελίσσεται με πολύ γρήγορους ρυθμούς. Υπάρχουν πολλά υπό μελέτη νέα φάρμακα για διάφορες γονιδιακές μεταλλάξεις και πρωτεΐνες που στοχεύουν στην αδρανοποίηση των καρκινικών κυττάρων και τον έλεγχο της ανάπτυξης του όγκου. Ακόμα και αν ο ασθενής φέρει μία μετάλλαξη στον όγκο για την οποία δεν υπάρχει κάποια ειδική θεραπεία ακόμη, είναι πιθανό να μπορεί να ενταχθεί σε κάποια κλινική μελέτη με σκοπό τη χορήγηση ενός υπό ανάπτυξη φαρμάκου.
Ακτινοθεραπεία
Κλινικές μελέτες
Η κλινική μελέτη είναι ένα είδος επιστημονικής έρευνας που στοχεύει στην αξιολόγηση των αποτελεσμάτων κάθε καινούριας ιατρικής προσέγγισης (π.χ. απεικονιστική εξέταση, καινούριο φάρμακο, εμβόλιο) τόσο στο χώρο της πρόληψης μίας νόσου όσο και στη διάγνωση και θεραπεία της. Κάθε κλινική μελέτη έχει συγκεκριμένο σκοπό και καλείται να απαντήσει σε συγκεκριμένα ιατρικά, επιστημονικά ερωτήματα.
Υπάρχουν πολλά είδη κλινικών μελετών που αφορούν τον καρκίνο. Εν συντομία είναι τα ακόλουθα:
Κλινικές μελέτες πρόληψης: αφορούν νέες προσεγγίσεις που μπορούν να μειώσουν τον κίνδυνο εμφάνισης καρκίνου (πχ διαιτητικές αγωγές).
Κλινικές μελέτες προσυμπτωματικού ελέγχου (screening trials): αφορούν μεθόδους που μας βοηθούν στην πρώιμη διάγνωση του καρκίνου, πριν αυτός δώσει συμπτώματα. Σε αυτές τις μελέτες συμμετέχουν υγιείς εθελοντές.
Κλινικές μελέτες διάγνωσης: αφορούν σε νέες διαγνωστικές προσεγγίσεις που επιτρέπουν τη γρήγορη, εύκολη, αναίμακτη και κυρίως αξιόπιστη, διάγνωση του καρκίνου. Σε αυτές τις μελέτες συμμετέχουν κυρίως εθελοντές που έχουν συμπτώματα συμβατά με καρκίνο.
Κλινικές μελέτες θεραπείας: αφορούν στην αξιολόγηση νέων θεραπευτικών χειρισμών, δηλαδή νέα φάρμακα, συνδυασμούς παλαιότερων και νεώτερων θεραπειών, νέα δοσολογικά σχήματα ή τον συνδυασμό διαφορετικών θεραπειών, όπως για παράδειγμα χημειοθεραπεία ταυτόχρονα με ακτινοβολία. Στόχος τους είναι η αποτελεσματικότερη θεραπεία του καρκίνου με τις λιγότερες δυνατές παρενέργειες. Συμμετέχουν μόνο ασθενείς που πάσχουν από καρκίνο.
Κλινικές μελέτες υποστηρικτικής αγωγής: αφορούν στην αξιολόγηση θεραπευτικών χειρισμών που στοχεύουν στην βελτίωση της ποιότητας ζωής των ασθενών με καρκίνο. Προσπαθούν να βρουν τρόπους για να βοηθήσουν τους ασθενείς να αντιμετωπίσουν τα συμπτώματα που προέρχονται από την ασθένεια τους ή τη θεραπεία που λαμβάνουν (πχ πόνος, ανορεξία, έμετοι κα). Συμμετέχουν μόνο ασθενείς που πάσχουν από καρκίνο.
Κλινικές μελέτες στον καρκίνο πνεύμονα
Ο ρόλος των κλινικών μελετών στον καρκίνο του πνεύμονα είναι πολύ σημαντικός. Ιδιαίτερα σημαντικός είναι ο ρόλος τους στην εμφάνιση νέων φαρμάκων για τη θεραπεία του καρκίνου του πνεύμονα, τόσο για την αύξηση της επιβίωσης των ασθενών, όσο και για τη βελτίωση της ποιότητας ζωής τους. Ένα νέο φάρμακο (πειραματικό) είναι το φάρμακο που δεν έχει πάρει έγκριση από τον Ελληνικό Οργανισμό Φαρμάκων (ΕΟΦ) για την συγκεκριμένη κακοήθεια ως καθιερωμένη θεραπεία και μπορεί να δοθεί σε ασθενείς μόνο στα πλαίσια κλινικών μελετών.
Οι κλινικές μελέτες στην ογκολογία διεξάγονται σε τρεις κυρίως φάσεις.
Κλινικές μελέτες φάσης Ι: πρόκειται για το πρώτο στάδιο των κλινικών μελετών, κατά το οποίο ένα νέο φάρμακο, που έχει περάσει τους προκλινικούς ελέγχους με επιτυχία, δοκιμάζεται σε ανθρώπους. Στόχος είναι η επίτευξη της ασφαλέστερης δοσολογίας και του αποτελεσματικότερου τρόπου και χρόνου χορήγησης του νέου φαρμάκου. Συνήθως, τέτοιες μελέτες δεν διεξάγονται στην Ελλάδα.
Κλινικές μελέτες φάσης ΙΙ: πρόκειται για τη δεύτερη φάση των κλινικών μελετών. Ελέγχουν τόσο την ασφάλεια όσο και την αποτελεσματικότητα της καινούριας θεραπείας. Κύριος σκοπός των μελετών αυτών είναι παρακολούθηση της δράσης του νέου φαρμάκου στον ανθρώπινο οργανισμό.
Κλινικές μελέτες φάσης ΙΙΙ: στην τρίτη φάση των κλινικών μελετών, το καινούριο φάρμακο συγκρίνεται με την καθιερωμένη έως τώρα θεραπεία για το συγκεκριμένο νόσημα. Οι μελέτες αυτές συμπεριλαμβάνουν μεγάλο αριθμό ασθενών, είναι συνήθως πολυκεντρικές, δηλαδή συμμετέχουν σε αυτές ασθενείς από πολλά ογκολογικά κέντρα και είναι συνήθως διεθνείς, δηλαδή διεξάγονται ταυτόχρονα σε πολλές χώρες.
Κλινικές μελέτες φάσης IV: Όταν το υπό μελέτη φάρμακο περάσει επιτυχώς και από την τρίτη φάση δοκιμής μπορεί ο πλήρης φάκελος του να κατατεθεί στον Εθνικό Οργανισμό φαρμάκων (ΕΟΦ) για την έγκρισή του ως καθιερωμένη θεραπεία. Η παρακολούθηση φαρμάκου δεν σταματά και μετά την έγκριση του από τον ΕΟΦ και αρχίζει τότε η μελέτη φάσης IV, που κύριος σκοπός της είναι η συνεχής παρακολούθηση των πιθανών παρενεργειών του φαρμάκου.
Συμμετοχή σε κλινική μελέτη
Ένας ασθενής με καρκίνο του πνεύμονα που συμμετέχει σε κλινική μελέτη συνεισφέρει αφενός στην επιστημονική και την κοινωνική πρόοδο, έχει όμως επιπλέον και πιθανό προσωπικό όφελος: Έχει πρόσβαση σε νέες πολλά υποσχόμενες θεραπείες που δεν θα είχε αλλιώς. Το υπό μελέτη φάρμακο μπορεί να αποδειχτεί πιο αποτελεσματικό από την καθιερωμένη θεραπεία και ο εθελοντής-ασθενής να είναι ο πρώτος που θα ωφεληθεί. Οι ασθενείς που συμμετέχουν σε κλινικές μελέτες παρακολουθούνται πιο στενά και πιο συχνά από εξειδικευμένη ιατρική και νοσηλευτική ομάδα και ασθενής δεν έχει καμία οικονομική επιβάρυνση ο ίδιος ή το ασφαλιστικό του ταμείο.
Η συμμετοχή σε κάποια κλινική μελέτη για τον καρκίνο του πνεύμονα δεν είναι ελεύθερη κινδύνων, αν και οι κίνδυνοι αυτοί είναι πολύ μικροί λόγω της στενής και συχνής παρακολούθησης των ασθενών. Υπάρχει πιθανότητα το υπό δοκιμή νέο φάρμακο ή υπό δοκιμή νέα θεραπεία να μην είναι καλύτερη από την καθιερωμένη. Υπάρχει πιθανότητα να εμφανιστούν μη αναμενόμενες ανεπιθύμητες ενέργειες. Χρειάζονται επίσης περισσότερες επισκέψεις στο νοσοκομείο από τις καθιερωμένες, γεγονός που μπορεί να δυσκολεύει κάποιους ασθενείς που διαμένουν σε απομακρυσμένες περιοχές.
Για τη συμμετοχή οποιουδήποτε ανθρώπου, υγιή ή ασθενή σε αντίστοιχη κλινική μελέτη, είναι απαραίτητη προϋπόθεση συγκατάθεσή του μετά από πλήρη ενημέρωση αυτού για τις λεπτομέρειες της μελέτης. Για το σκοπό αυτό, πάντα προηγείται η συμπλήρωση και υπογραφή ενός εντύπου συγκατάθεσης. Το έντυπο συγκατάθεσης παρέχει πληροφορίες στον συμμετέχοντα σχετικά με το σκοπό διεξαγωγής της δοκιμής αυτής, τα πιθανά οφέλη και τους πιθανούς κινδύνους, τις διαδικασίες που θα ακολουθηθούν κατά τη διάρκεια της μελέτης και τις υποχρεώσεις του ασθενούς. Ένας ασθενής που θα συμφωνήσει να συμμετάσχει σε μία κλινική μελέτη μπορεί να αποχωρήσει από αυτή οποιαδήποτε στιγμή επιθυμεί χωρίς αυτό να σημαίνει ότι θα σταματήσει η παρακολούθησή του από το ογκολογικό τμήμα ή ότι δε θα λάβει άλλη θεραπεία.
Μετά το τέλος της κλινικής μελέτης, οι ασθενείς που συμμετείχαν σε αυτήν παρακολουθούνται για ένα συγκεκριμένο χρονικό διάστημα που ορίζεται κάθε φορά από τον σχεδιασμό της μελέτης. Δεν υπάρχουν δεσμεύσεις όσον αφορά την περαιτέρω θεραπεία και παρακολούθηση των ασθενών.

